Startseite - Forschung und Lehre - Neurologie
Neurologie
Die Universitätsklinik für Neurologie am Evangelischen Krankenhaus Oldenburg behandelt alle neurologischen Erkrankungen des Nervensystems und der Muskulatur. Zur raschen Versorgung von Schlaganfallpatienten steht eine spezialisierte Stroke Unit zur Verfügung, während für Patienten mit schweren und hochkomplexen Erkrankungen eine neurologisch-internistische Intensivstation vorgehalten wird. Die ambulante Versorgung erfolgt in der Neurologischen Hochschulambulanz im Medizinischen Versorgungszentrum (MEVO).
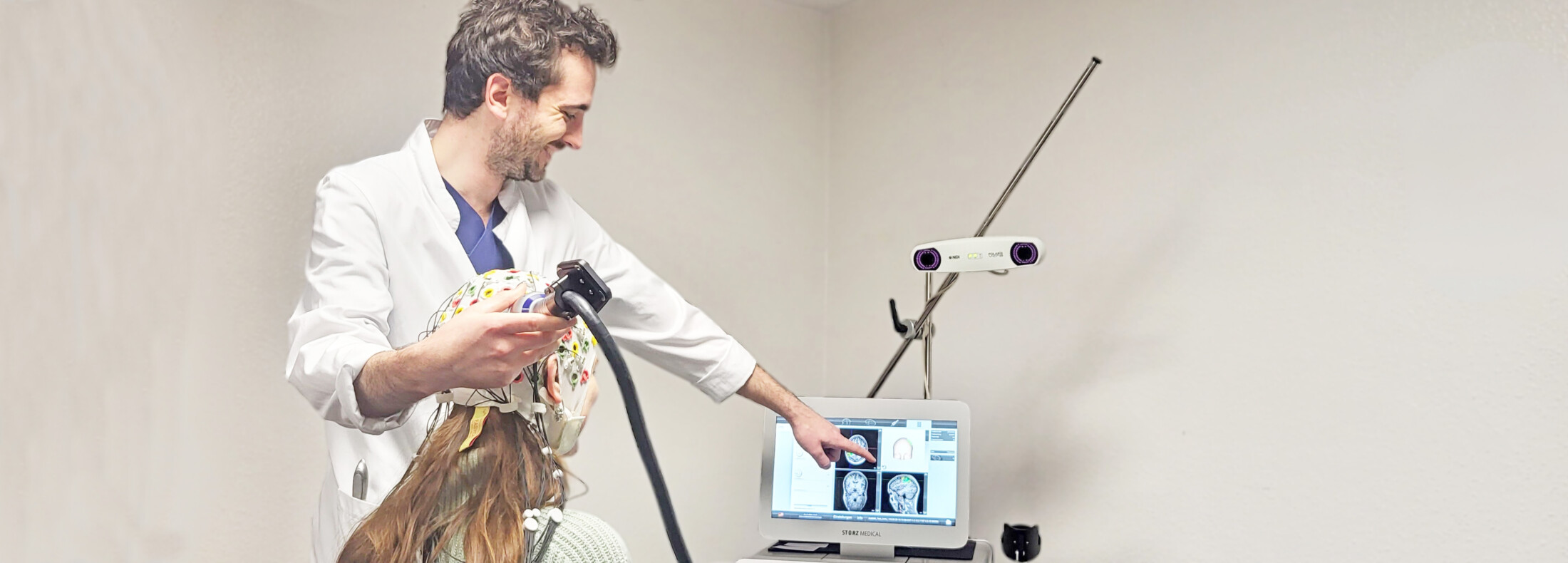
Der Schwerpunkt unserer Forschung liegt in der kognitiven Neurologie, das heißt, wir beschäftigen uns mit kognitiven Veränderungen, die im Rahmen neurologischer Erkrankungen auftreten. Wir setzen dabei verschiedene Methoden ein, die von klinischen Studien bis hin zu hochauflösendem EEG und funktioneller Bildgebung reichen, das heißt, wir untersuchen Veränderungen der höheren Hirnleistungen, die im Rahmen einer neurologischen Erkrankung auftreten, mit naturwissenschaftlichen Methoden.
Derzeit haben wir drei Schwerpunkte:
Wie Bewegungsstörungen kognitive Kontrollmechanismen beeinflussen.
Wie der Energiestoffwechsel des Körpers kognitive Kontrollmechanismen beeinflusst.
Wie Demenzerkrankungen früher und besser klassifiziert werden können.
In weiteren Studien untersuchen wir die zerebrale Hämodynamik nach Schlaganfall und die Immunantwort bei entzündlichen Hirnerkrankungen wie der Multiplen Sklerose.
Wir geben Ihnen hier einen Einblick in unsere Arbeit, wir verbinden klinische und forschende Tätigkeit, weil wir der festen Überzeugung sind, dass klinische und grundlagenwissenschaftliche Ausrichtung zielführend zusammenwirken, um Ergebnisse zu erzielen, die der Therapie und auch der Lebensqualität unserer Patienten zugutekommen.
Die wissenschaftlichen Schwerpunkte der Universitätsklinik für Neurologie liegen in den Bereichen Bewegungsstörungen und kognitive Neurologie.
Aktuelle Forschungsthemen sind
- Gedächtnisstörungen bei Morbus Parkinson: Einfluss von Schlaf und Kognition und Auswirkungen auf den Alltag
- Interaktion von Emotion und Kognition auf motorische Prozesse
- Neurofeedback zur Behandlung des Morbus Parkinson
- Transkutane Stimulation des N. vagus zur Behandlung von kognitiven Störungen und Gangstörungen bei Morbus Parkinson
- Transkranielle AC-Stimulation (tACS) zur Behandlung von Bewegungsstörungen bei Morbus Parkinson
- Nahinfrarotspektroskopie (NIRS) bei der Behandlung des ischämischen Schlaganfalls